原子核由质子和(除了大部分氢之外)中子组成。质子的数量决定了它是什么元素:氧有8个质子,铁有26个,黄金有79个。然而,中子的数量是会变革的。如果两个原子都有相同数量的质子和中子,那它们是同一同位素。如果它们有相同数量的质子和不同数量的中子,那它们便是同一元素的不同同位素。同位素通过元素、中子和质子的总数来标识。
有些同位素是稳定的:只要什么事情都不发生,比如与经由的中子相遇,它们将在全体宇宙的寿命内持续存在。然而,大多数元素有多种不稳定的同位素,它们会随着韶光逐步衰变,开释辐射并变成完备不同的东西。

例如,碳的最常见同位素是碳-12,由六个质子和六个中子组成。这对付稳定来说是一个得当的平衡,每个碳-12原子在大多数环境中都会永久存不才去。这对我们来说是件好事,由于我们体内一种最常见的元素是放射性的话就会有问题。碳-13,带有第七个中子,形成更少但同样稳定。
然而,自然界中也存在碳-14,我们可以在实验室制造碳-11。这两者都是放射性的,意味着它们会衰变,但碳-11会更快。这便是半衰期的观点发挥浸染的地方。
任何单个原子衰变所需的韶光是无法预测的,但对付大样本的统计预测可以非常准确。
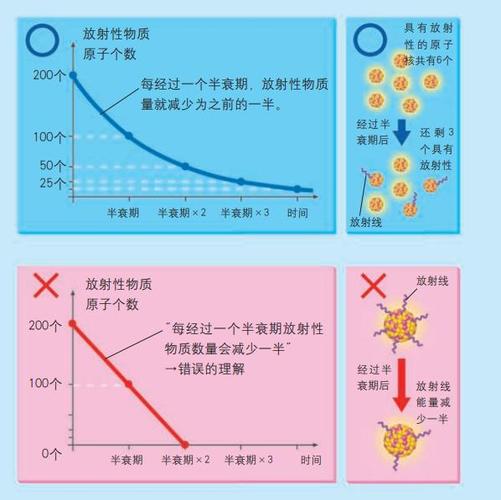
对付任何放射性同位素的大样本来说,这种同位素的半衰期期间内一半的原子会衰变。如果你适当地储存一公斤的碳-14,5700年后,你的后代会拥有500克碳-14和500克氮-14。在此期间,大量的贝塔粒子(快速移动的电子)将会被开释,由于一半的原子从一种原子变成另一种原子。
另一方面,一半碳-11样本将在短短20分钟内转变成硼-11,这便是为什么我们必须自己制造它。任何自然形成的碳-11都会很快衰变。
你可能期望在其余5700年后,剩下的碳-14也都会衰变,只留下氮,但事实并非如此。相反,在此期间会有一半剩余的碳-14会衰变,留下250克。再经由5.7千年,只剩下125克,依此类推。
只有当数百万年过去时,当你的末了几个碳原子时,变得难以预测 - 由于样本尺寸非常小,你可能会失落客岁夜部分剩余的碳,乃至少于一半,只管一半是最有可能的结果。
从科学角度来看,半衰期对付我们能够确定物体年事至关主要。植物和光合浸染的藻类从大气中接管碳,个中包含与大气中存在量成比例的少量碳-14。直到最近,这意味着活植物组织中的碳-14,并且那些以这些植物为食品的生物中的碳-14是恒定的。然而,一旦植物或动物去世亡,碳-14开始衰变,而碳-12和-13保持不变。如果你找到一个物体,其相对付稳定碳同位素在历史大气中的数量只有一半,意味着它有5700年的历史。相对付浓度,碳-14数量只有四分之一意味着它有10400年的历史。
通过丈量碳-14的数量,我们首次能够为我们先人的化石确定年事,这是理解我们的进化的主要一步。它也被用于验证声称是古代文物的物体的真实性。
然而,碳测年法也有其局限性。它不能用于丈量数百万年的物体年事,由于剩余的碳-14会非常少。另一方面,近年来人类影响了大气中的碳比例。以前,大部分碳-14是通过宇宙射线撞击大气氮原子产生的。燃烧化石燃料开释的碳险些没有碳-14,从而降落了大气比例,而核试验产生了足够多的碳-14以提高环球均匀比例。这两种人类活动相互浸染,但两者都改变了比例,在未来只用碳将会很难估计我们时期物体的年事。
然而,幸运的是,还有很多其他放射性同位素可用于测年,个中一些衰变速率慢得多,使我们能够估计更古老物体的年事。
由于碳-14的半衰期为数千年,每年仅有少量碳-14原子衰变,我们不会因其存在于我们的器官中而受到太大影响。然而,对付一些半衰期较短的同位素而言则并非如此。例如锶-90、铯-137和钴-60等同位素半衰期很短,衰变时会开释大量辐射,但足够长,使得当意外事宜导致它们开释时我们不能轻易等待辐射消逝。当它们衰变开释的辐射足够强大以至于构成危险时,这便成为一个严重问题。
另一方面,具有较短半衰期的同位素也可以有用。我们用它们进行医学成像,通过追踪它们开释的辐射来识别人体问题,或开释我们须要的粒子用于科学实验。常日情形下,主要的是探求一个适宜事情的半衰期的同位素。
半衰期观点还可以运用到其他方面。药物、维生素和毒药在体内都有一个半衰期,个中有一半在特定时间内被渗出或分解。对付前两者,这使我们能够打算我们须要多快更换它们。










